作者:kelly
一、共价键和共价化合物
共价键:原子间通过共用电子对所形成的相互作用
两个原子之间共享一个或者对各电子对
成键元素:一般是同种或者不同种的非金属元素
条件:原子最外层电子未达到稳定状态
分类:
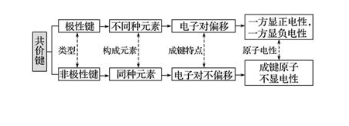
共价化合物
以共用电子对形成的分子化合物
常见共价化合物:
非金属氢化物:H2O,H2S
非金属氧化物:CO,CO2,SO2
含氧酸:H2SO4,HNO3
大多数有机化合物:CH4,CH3CH2OH
共价分子的表示方法和形成过程

二、化学键与分子间作用力
化学键:
相邻的原子之间的相互作用
分类:
离子键:带相反电荷例子之间的相互作用,阴阳离子直接通过静电作用形成的化学键,一般是活泼的金属原子和非金属原子
共价键:原子间通过共用电子对所形成的相互作用
极性键:电子对偏移,氢键,酸碱键,链接键,偶极键,硫醇键
非极性键:电子对不偏移:C-C, C-H, N-N, S-S,Cl-Cl
化学反应
定义:反应物中的原子重新组合为产物分子的一种过程,在化学反应中,包含着反应物内化学键的断裂和产物分子化学键的形成
本质:旧化学键的断裂和新化学键的形成
分子间作用力
定义:分子之间存在一种把分子聚集在一起的作用力,也叫范德华力
范德华力比化学键弱的多,主要影响物质的熔点,沸点等
氢键:
一种分子间的作用力,比化学键弱,比范德华力强
氢键会使物质的熔点和沸点升高,由于固体融化或液体汽化是必须破坏分子间的氢键,消耗较多能量
上一篇:常见的物质颜色和实验仪器
下一篇:没有了!
发表评论:
评论记录: